


 |
Hoje é Sexta-feira, 27 de Fevereiro de 2026.
|
Hoje é Sexta-feira, 27 de Fevereiro de 2026. 


 |
Hoje é Sexta-feira, 27 de Fevereiro de 2026.
|
Hoje é Sexta-feira, 27 de Fevereiro de 2026. 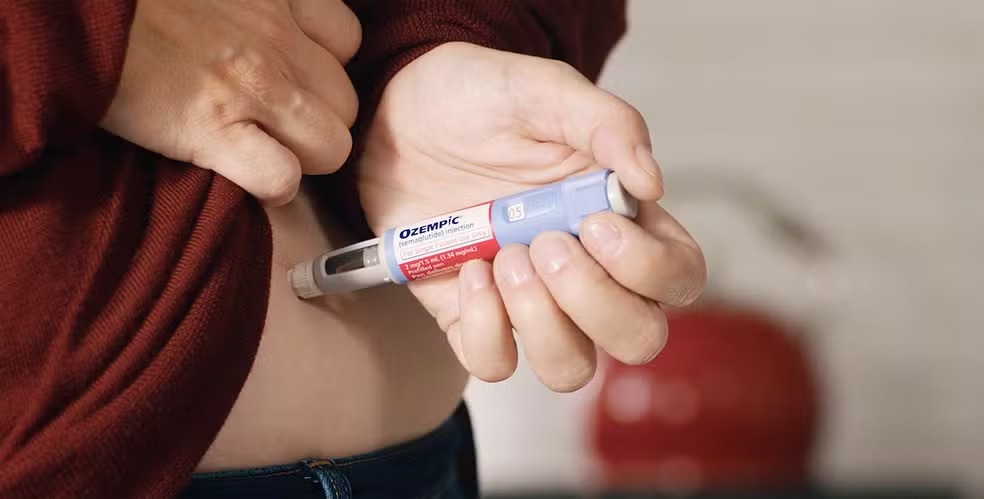

O Superior Tribunal de Justiça (STJ) decidiu por unanimidade negar o pedido da farmacêutica Novo Nordisk para estender a patente da semaglutida no Brasil, princípio ativo dos medicamentos Ozempic e Rybelsus. Com a decisão, fica mantido o prazo original de validade da patente, que expira em março de 2026.
A semaglutida é um medicamento que imita o hormônio GLP-1, produzido naturalmente pelo intestino, e atua no cérebro reduzindo o apetite. Ela é indicada para o tratamento do diabetes tipo 2 e da obesidade, sendo comercializada na forma injetável, como o Ozempic, e em comprimidos, como o Rybelsus.
A decisão é considerada relevante porque impede que a exclusividade da Novo Nordisk fosse prorrogada até 2038, o que atrasaria por mais de uma década a entrada de versões genéricas e similares no mercado brasileiro. A farmacêutica alegava que houve demora do Instituto Nacional da Propriedade Industrial (INPI) na análise do pedido de patente e que esse período deveria ser compensado com a extensão do prazo.
O STJ rejeitou o argumento ao aplicar entendimento já consolidado pelo Supremo Tribunal Federal (STF) em 2021, segundo o qual não existe previsão legal para prorrogar patentes no Brasil em razão de atrasos administrativos. Pela legislação, a proteção é de 20 anos, sem exceções.
Apesar da decisão, os genéricos não poderão ser comercializados de forma imediata. A patente segue válida até março de 2026 e, somente após esse prazo, outros laboratórios poderão vender versões concorrentes, desde que obtenham aprovação da Agência Nacional de Vigilância Sanitária (Anvisa).
Especialistas indicam que a entrada de genéricos tende a reduzir os preços em cerca de 30% ou mais, dependendo do grau de concorrência. Atualmente, uma caneta de semaglutida custa em torno de R$ 1 mil no mercado brasileiro.
Para o Sistema Único de Saúde (SUS), o impacto potencial é significativo. Hoje, não há medicamentos específicos para obesidade disponíveis na rede pública, principalmente devido ao alto custo. Segundo o Ministério da Saúde, a incorporação da semaglutida custaria cerca de R$ 8 bilhões por ano, valor próximo ao dobro do orçamento do programa Farmácia Popular. Com genéricos mais baratos, a inclusão do tratamento passa a ser considerada mais viável.
O Ministério da Saúde informou que já solicitou à Anvisa prioridade na análise de cerca de 20 novos pedidos de canetas de semaglutida e liraglutida. O objetivo é que, quando a patente expirar, haja múltiplas opções no mercado, favorecendo a concorrência e a queda de preços. Em nota, a pasta destacou que a redução média de 30% nos preços, observada com a entrada de genéricos, é fator determinante para avaliar a incorporação desses medicamentos ao SUS.
O tema ganha ainda mais relevância diante do cenário da obesidade no Brasil. Atualmente, sete em cada dez adultos estão acima do peso e 31% já são considerados obesos, com crescimento mais acelerado entre a população dependente do SUS. Hoje, o tratamento público se concentra nas doenças associadas, como diabetes e hipertensão, e não na obesidade em si. A única alternativa terapêutica disponível é a cirurgia bariátrica, cujo acesso é limitado, com apenas cerca de 10% dos procedimentos realizados pelo SUS.
Especialistas defendem a possível adoção das canetas no sistema público, mas ressaltam que o medicamento deve fazer parte de uma estratégia mais ampla, com critérios rigorosos e acompanhamento multiprofissional, já que a obesidade é uma doença multifatorial.
Por outro lado, representantes da indústria farmacêutica criticam a decisão, afirmando que a impossibilidade de extensão reduz o tempo efetivo de proteção das patentes em países onde o exame é mais lento, o que poderia desestimular investimentos em inovação no Brasil.
Até março de 2026, o mercado permanece sob exclusividade da Novo Nordisk. Nesse período, Anvisa, Ministério da Saúde e laboratórios nacionais se preparam para o cenário pós-patente. Empresas como a EMS já afirmaram que a manutenção do prazo original garante segurança jurídica para desenvolver e comercializar medicamentos à base de semaglutida após o vencimento da patente, desde que cumpridas as exigências regulatórias. Com informações: g1
